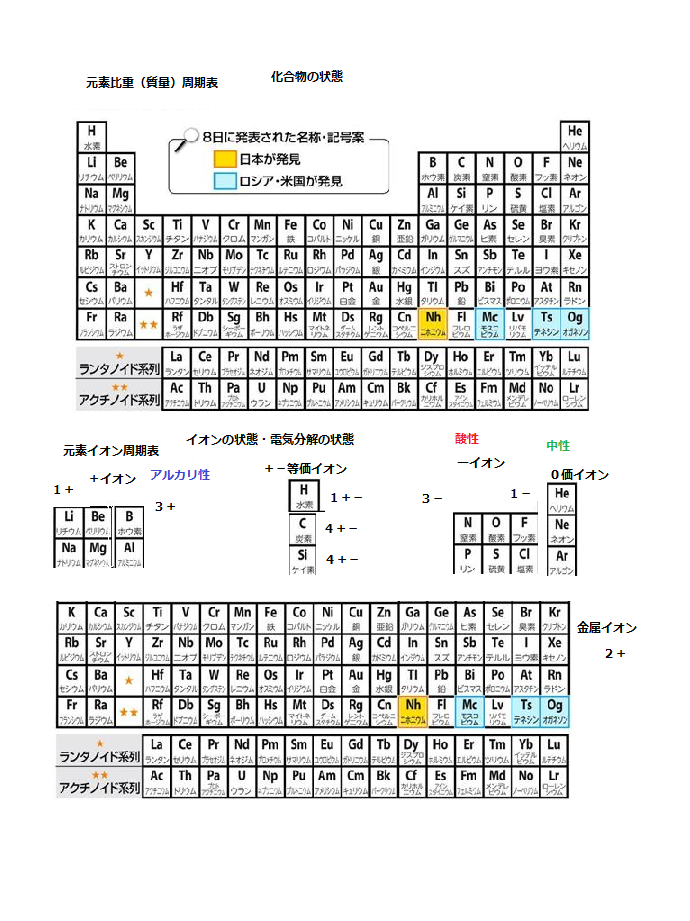
比重・イオン周期表
1.比重(質量)周期表
化合物(+イオンとーイオンが混在している状態)の時、これを使用。
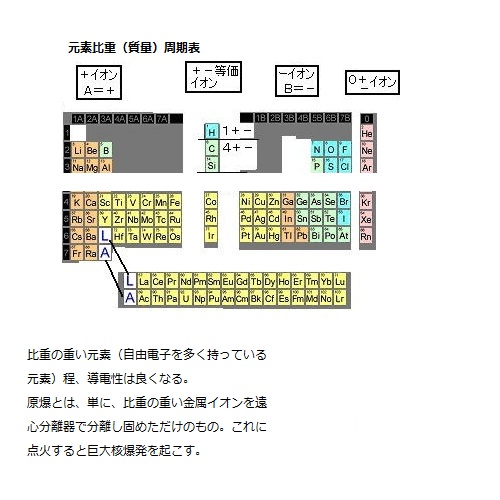

2.イオン化・電気分解
イオン化―水に溶けて目に見えなくなった状態
電気分解―+イオンとーイオンを分けて、取り出す状態(高分子+イオン・-イオン状態)
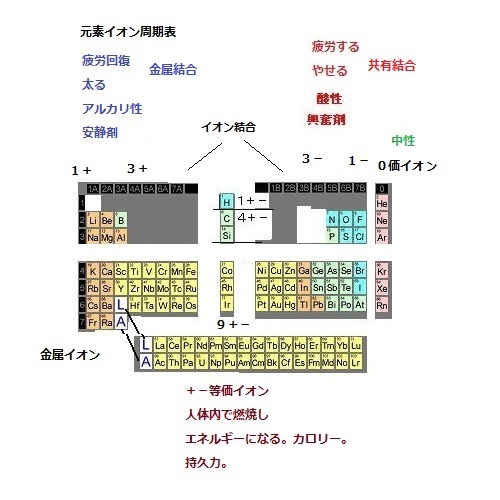
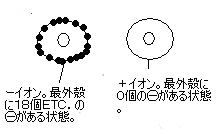
3.砂糖(炭素C4+-を水HOに溶かしたもの)は酸性にもアルカリ性にもなる。0価イオンが中性。
4.金属イオンはほぼすべて2+イオンとされているが、毒薬Asヒ素・カドミウムCd(重金属でもある)・水銀Hg(重金属でもある)はーイオンの所にあり、同じ周期のカリウムK+、カルシウムCa2+は安静剤として人体に有用。また、同じ周期の鉄Fe 銅Cu 亜鉛Znは+-等価イオンの所にあり、人体でO2―をひっつけたり離したりする重要な元素。
また、半導体(ダイオード、トランジスタ、太陽電池、磁石(ニッケル・コバルト)、100円ライターの発火電池等)は、+イオン金属とーイオン金属を貼り合わせただけのもの。つまり、金属イオンがすべて2+であれば作れない。この事からも、金属イオンも1+~8+、9+-、8-~1-になっていると分かります。あしからず。
上記より、金属イオンにも電価があり、+イオン(アルカリ性)金属・+-等価イオン(中性)金属・-イオン(酸性)金属があるように見える。
なお、猛毒の青酸はHCN、つまり、窒素N3-と+-等価イオン。+イオンが爆弾・-イオンが毒薬。